2020-07-03 09:51:49 | 2103 次浏览
今天,上海科技大学又传来捷报:北京时间7月1日,上海科技大学iHuman团队刘志杰及华甜等在Nature 在线发表题为“Structural basis of CXC chemokine receptor 2 activation and signalling”的研究论文,该研究报告白细胞介素8激活的人类CXC趋化因子受体2(CXCR2)与Gi蛋白复合的冷冻电子显微镜结构。
自今年1月15日至今,在短短半年的时间内,上科大已经在Nature、Cell、Science上上刊登了多达12篇论文。几乎是平均每半个月出一篇顶刊,完全“秒杀”各大老牌名校。
2020年5月22日,上海科技大学饶子和、王权及中国科学院武汉病毒研究所龚鹏共同通讯在Cell 在线发表题为“Structural basis for RNA replication by the SARS-CoV-2 polymerase”的研究论文,该研究解析了RNA聚合酶及其辅助因子与RNA和抗病毒候选药物瑞德西韦复合体2.9 Å的三维结构,揭示了新型冠状病毒聚合酶复合体催化过程中“转位前”和“转位后”两个生理状态的构象特征。
2020年4月29日, 清华大学祁海、上海科技大学胡霁、清华大学钟毅共同通讯在Nature 在线发表题为“Brain control of humoral immune responses amenable to behavioural modulation”的研究论文,该研究发现了第一条由神经信号传递(非内分泌激素介导)的中枢神经对适应性免疫应答进行调控的解剖学明确的通路,该研究揭示了大脑对适应性免疫的控制,并提出了通过行为干预增强免疫能力的可能性。
2020年4月29日, 普渡大学窦乐添、Brett Savoie和上海科技大学于奕共同通讯在Nature 在线发表题为“Two-dimensional halide perovskite lateral epitaxial heterostructures”的研究论文,该研究在新型半导体异质结研究中取得重要进展,首次成功制备并表征了二维卤化物钙钛矿横向外延异质结。这些发现为卤化钙钛矿半导体的固定化和稳定化提供了见识,并展示了用于复杂和分子薄的超晶格,器件和集成电路的材料平台。
2020年4月24日,上海科技大学Raymond C. Stevens及密歇根大学Roger D. Cone共同通讯在Science 在线发表题为“Determination of the melanocortin-4 receptor structure identifies Ca2+ as a cofactor for ligand binding”的研究论文,该研究首次解析人源黑皮质素-4-受体(MC4R)与环形多肽配体SHU9119复合物2.8埃分辨率的晶体结构。该研究首次观察到功能性Ca2+与GPCR的结合模式,发现Ca2+有助于稳定受体-候选药物复合物,并使内源性激动剂α-黑素细胞刺激激素的亲和力和效力得到了极大的提高。总而言之,该成果对于开发针对此受体的肥胖症药物有重要的参考价值。 最后,Science 发表了题为“Calcium as a biased cofactor”的点评文章,系统总结了该研究成果。
2020年4月23日,上海科技大学,南开大学,清华大学,中科院生物物理所,伯明翰大学等多单位合作,饶子和,王权,李俊及Gurdyal S. Besra及共同通讯在Science 在线发表题为“Structures of cell wall arabinosyltransferases with the anti-tuberculosis drug ethambutol”的研究论文,该研究确定了分枝杆菌EmbA-EmbB和EmbC-EmbC配合物在其糖基供体和受体底物以及乙胺丁醇存在下的冷冻电子显微镜和X射线晶体结构。 该研究工作为理解生化功能和抑制阿拉伯糖基转移酶以及开发新的抗结核药物提供了结构基础。
2020年4月22日,中国科学院上海药物研究所柳红/许叶春,上海科技大学杨海涛及中国科学院武汉病毒所张磊砢共同通讯在Science 在线发表题为”Structure-based design of antiviral drug candidates targeting the SARS-CoV-2 main protease“的研究论文,该研究设计并合成了两种针对 Mpro的先导化合物(11a和11b)。两者均表现出优异的抑制活性和有效的抗SARS-CoV-2感染活性。SARS-CoV-2Mpro与11a或11b形成复合物的X射线晶体结构均以1.5分辨率测定,表明11a和11b的醛基共价键合到Mpro的Cys145。两种化合物在体内均显示出良好的PK特性,而11a的毒性也较低,表明这些化合物是有前途的候选药物。
2020年4月10日,清华大学饶子和,娄智勇及上海科技大学王权共同通讯在Science 题为“Structure of the RNA-dependent RNA polymerase from COVID-19 virus”的研究论文,该研究报告了SARS-Cov-2辅助因子nsp7和nsp8与全长nsp12的cryo-EM结构,分辨率为2.9埃。除了病毒聚合酶家族的聚合酶核心的保守结构和冠状病毒RdRp中特有的与Nido RdRp相关的核苷酸转移酶(NiRAN)域外,nsp12在其N末端还拥有一个新鉴定的β-发夹结构域。观察到病毒复制和转录的关键残基。该研究还提供了比较分析,以显示瑞德昔韦如何与该聚合酶结合。这种结构提供了对冠状病毒复制/转录机制的核心组成部分的见解,并为设计针对病毒RdRp的新型抗病毒治疗药物提供了思路。
2020年4月9日,上海科技大学饶子和,杨海涛及中科院上海药物所蒋华良共同通讯在Nature 在线发表题为“Structure of Mpro from COVID-19 virus and discovery of its inhibitors”的研究论文,该研究解析了新型冠状病毒关键药物靶点——主蛋白酶(Mpro)的高分辨率三维空间结构,并综合利用三种不同的药物发现策略,找到针对新冠病毒的潜在药物。
2020年2月19日,上海科技大学徐菲,上海交通大学雷鸣和武健共同通讯在Nature 在线发表题为“Structural basis of ligand recognition and self-activation of orphan GPR52”的研究论文,该研究介绍了人类GPR52在无配体和Gs耦合状态下的高分辨率结构。结构表明,细胞外环2占据了正构结合袋,并作为内置的激动剂起作用,赋予GPR523高水平的基础活性。当在没有外部激动剂的情况下将Gs偶联至GPR52时,将达到完全激活状态。该受体还具有配体结合的侧袋。对GPR52的结构和功能的这些见解可以增进我们对其他自激活GPCR的理解,能够鉴定内源和工具配体,并指导靶向GPR52的药物发现工作。
2020年1月30日,上海科技大学刘志杰及华甜共同通讯在Cell 在线发表题为“Activation and Signaling Mechanism Revealed by Cannabinoid Receptor-Gi Complex Structures”的研究论文,该研究揭开了大麻素受体CB1和CB2分别处于拮抗状态、中间态及激活态的神秘面纱,对大麻素系统的认知又迈出了坚实的一大步。”华甜副研究员说。该研究发现,虽然在激动剂调控下CB1和CB2与下游Gi蛋白的接头方式非常相似,但是两个受体的激活机制却各不相同。另外,他们还首次发现胆固醇分子对CB1的别构调节功能,为靶向CB1受体的特异性药物设计提供了新思路。同时,该研究还揭示了CB2受体获得高选择性配体的分子机制,为针对CB2的免疫类新药设计提供了更加精确的分子模型和理论基础。
2020年1月15日,同济大学戈宝学及上海科技大学饶子和共同通讯在Nature 在线发表题为“Host-mediated ubiquitination of a mycobacterial protein suppresses immunity”的研究论文,该研究发现宿主E3泛素连接酶ANAPC2(后期促进复合物/环体的核心亚基)与分枝杆菌蛋白Rv0222相互作用,并促进赖氨酸11连接的泛素链对Rv0222的赖氨酸76的附着,从而抑制促炎细胞因子的表达。总而言之,该研究发现确定了结核分枝杆菌用来抑制宿主免疫力的一种以前未被认识的机制,并提供了与开发针对结核分枝杆菌的有效免疫调节剂有关的见解。
而最新发表的这篇,是来自上海科技大学iHuman研究所的科研团队,他们在人体趋化因子系统信号转导研究领域取得重大突破,并成功破解了趋化因子受体CXCR2 (CXC chemokine receptor 2)与趋化因子白细胞介素IL8 (Interleukin 8)及下游信号转导分子G蛋白三元复合物的冷冻电镜结构,同时还解析了CXCR2与潜在癌症治疗药物分子复合物的晶体结构。
图1:IL8激活CXCR2趋化T细胞到癌细胞过程的艺术展示图(由Julie Liu设计绘制)
该项研究首次揭示内源性蛋白配体激活G蛋白偶联受体(GPCR)的新机制,为精准的新型抗癌药物设计开启新篇章。该成果以Structure basis of CXC chemokine receptor 2 activation and signaling为题。
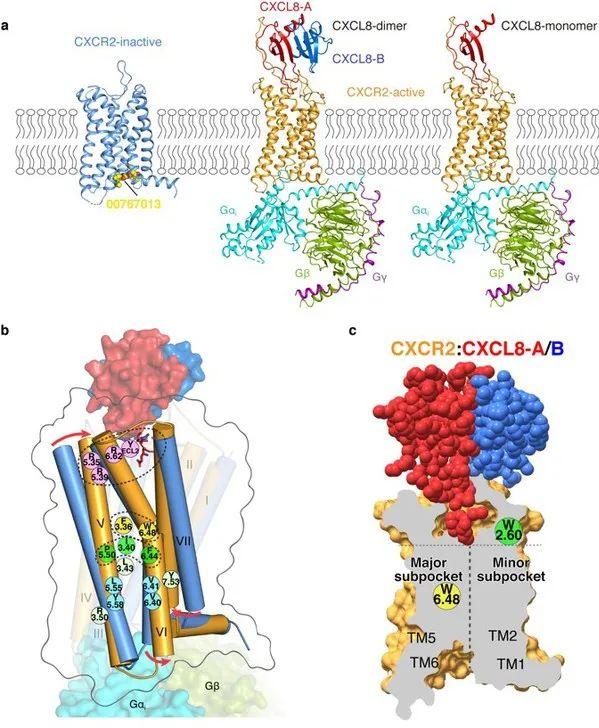
图2:(a) 分别与单体和二体IL8结合的CXCR2与Gi复合物的电镜结构,以及CXCR2与拮抗剂结合的晶体结构; (b) CXCR2的激活机制卡通展示图; (c) 与二体IL8结合的CXCR2结构剖面图。
上海科技大学(ShanghaiTech University),简称上科大(ShanghaiTech),实际真正成立也才仅6年,是一所由上海市人民政府与中国科学院共同举办、共同建设,由上海市人民政府主管的全日制普通高等学校;是教育部和上海市共建“国家教育综合改革试验区”的试点高校、张江综合性国家科学中心的组成部分;入选国家第二批大众创业万众创新示范基地、首批上海高等学校一流本科建设引领计划、首批上海高等学校一流研究生教育引领计划。学校位于上海—浦东新区—张江高科技园中区,以理工科为主,与中国科学院所属研究院所开展科教融合。
上海科技大学于2013年9月30日经教育部批准同意正式建立。2013年至2016年,学校与中国科学院大学联合招收了4届硕博连读研究生。2014年,开始招收本科生。从2017年起,学校可独立招收、培养硕士和博士研究生。2018年,学校获批成为博士、硕士学位授予单位。
据2020年4月学校官网显示,上海科技大学设有张江校区(校本部)和岳阳路校区,校本部占地约900亩,总建筑面积约70万平方米;学校下设5个学院,1个研究院,3个研究所;拥有1个博士后科研流动站,1个一级学科博士学位授权点,4个一级学科硕士学位授权点;在7个一级学科独立招收和培养硕士和博士研究生;开设9个本科专业。截至2019年10月底,学校已选聘493位教授(特聘教授282位,常任教授到位211位)。截至2019年9月,学校共有在籍学生3747人,其中本科生1550人,硕士研究生1459人,博士研究生738人;学校已建立249个研究组。
https://www.nature.com/articles/s41586-020-2492-5
http://www.shanghaitech.edu.cn/2020/0702/c1001a53449/page.htm
http://www.shanghaitech.edu.cn/2020/0629/c9a53356/page.psp
http://siais.shanghaitech.edu.cn/2020/0409/c5461a52659/page.htm
http://www.shanghaitech.edu.cn/2020/0409/c1001a51034/page.htm
http://www.shanghaitech.edu.cn/eng/2020/0216/c1688a50262/page.htm
本文由科研小助手(ID:SciRes)整理,转载请注明来源
本文转载仅仅是出于传播信息的需要,并不意味着代表本网站观点或证实其内容的真实性;作者如果不希望被转载或其他事宜,请与我们直接联系。如其他媒体、网站或个人从本网站转载使用文章,须保留本网站注明的“来源”,并自负版权等法律责任;凡注明来源为“辑思编译”的文章,如需转载,请注明来源editideas.cn/并附上文章链接。












